【摘要】 本文详细解析小动物活体成像原理、生物发光与荧光成像技术差异、常见问题解决方案。科学指南针提供专业活体成像服务及技术支持。

小动物光学活体成像,已经成为药物研发、肿瘤研究和分子示踪中的常用工具。但在实验中,你是否也遇到过这些问题:
明明打了探针,却几乎没有信号?
成像背景一片亮,根本分不清靶点?
同样的方案,别人能复现,你却总是失败?
很多时候,问题并不在仪器,而是在实验设计的第一步就埋下了隐患。本文将从成像原理出发,结合常见实验场景,系统梳理小动物光学活体成像中最容易踩坑、也最容易被忽略的关键点。
01小动物活体成像仪器原理
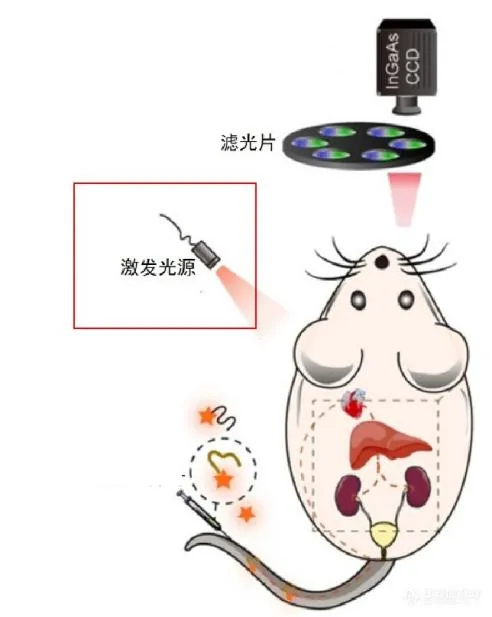
1. 高灵敏度制冷CCD/CMOS相机:核心“眼睛”,负责捕获微弱的光子信号并将其转换为电信号;深度制冷(如-80℃至-90℃)
2. 滤光片:分离特定波长光的“滤镜”
3. 激光器:提供高强度、单色性好的激发光,适用于特定波长的高效率激发(如532nm, 635nm, 808nm等
4. 密闭成像暗箱:为成像提供一个完全避光的环境,这是检测微弱信号(尤其是生物发光)的前提
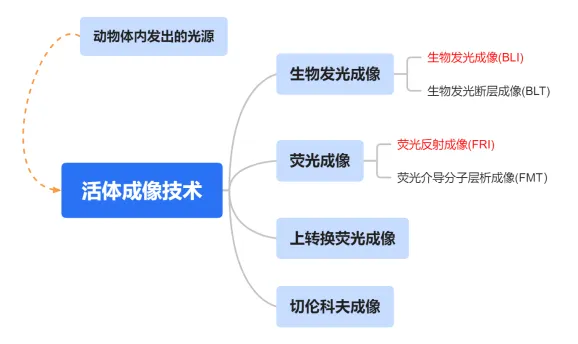
02小动物活体成像分类(生物发光/荧光)
根据动物体内发出的光源,光学成像可进行生物发光成像(Bioluminescence imaging,BLI)、荧光成像(Fluorescence imaging,FI)。
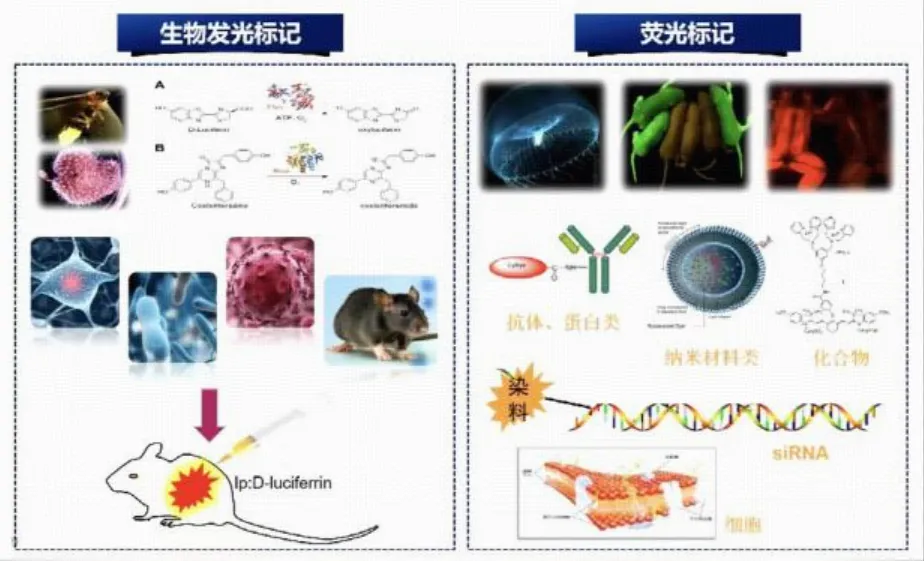
1、生物发光(BLI)成像
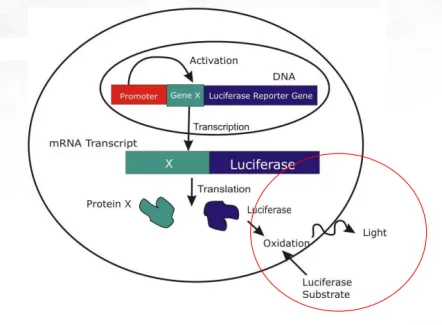
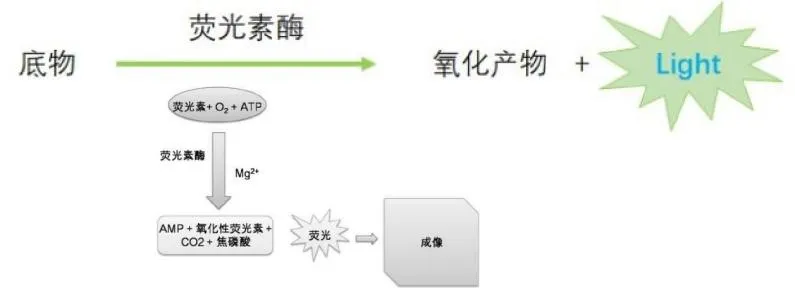
1.实验原理
BLI 技术原理:将荧光素酶基因连接于启动子下游,稳定整合到细胞染色体内,使萤光素酶在生物体内得到持续表达,注射底 物后与表达的萤光素酶反应发光。(自发光,其信号的发射不需要外部光源激发)
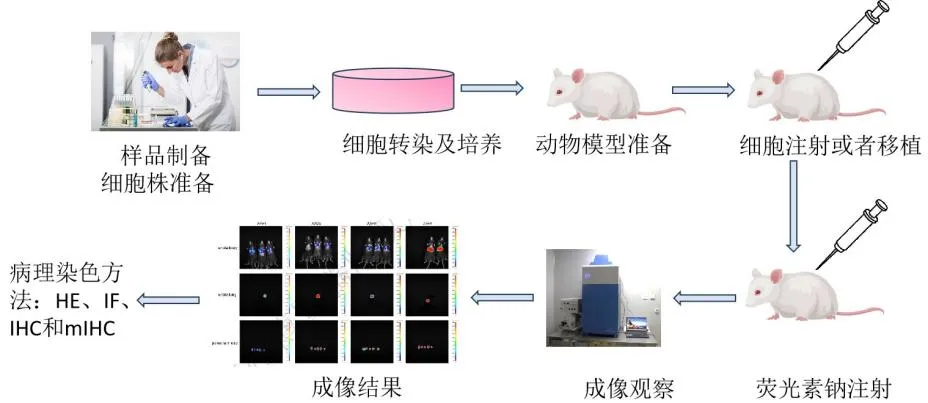
2.实验步骤
一个完整的生物发光活体成像过程包括构建荧光素酶重组质粒、细胞转染和筛选、荧光素酶活性鉴定阳性克隆,再将阳性克隆细胞移植到体内建立动物模型,进而通过小动物活体成像系统检测动物体内特定部位发出的荧光信号。最后取出肿瘤组织,通过染色进行病理形态学分析。
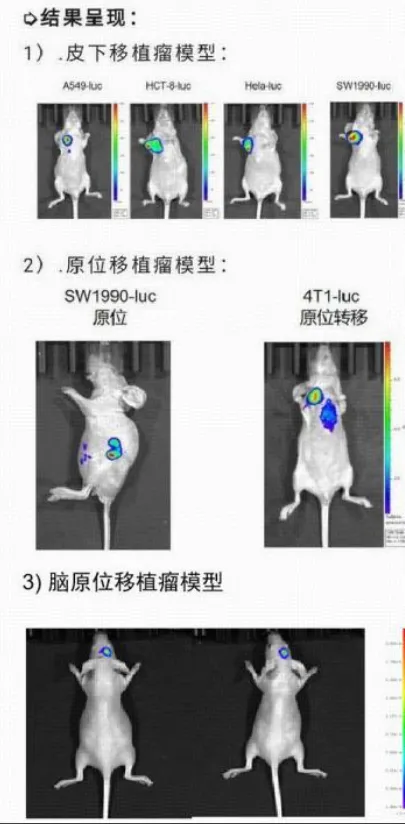
3.模型的选择

2、荧光成像
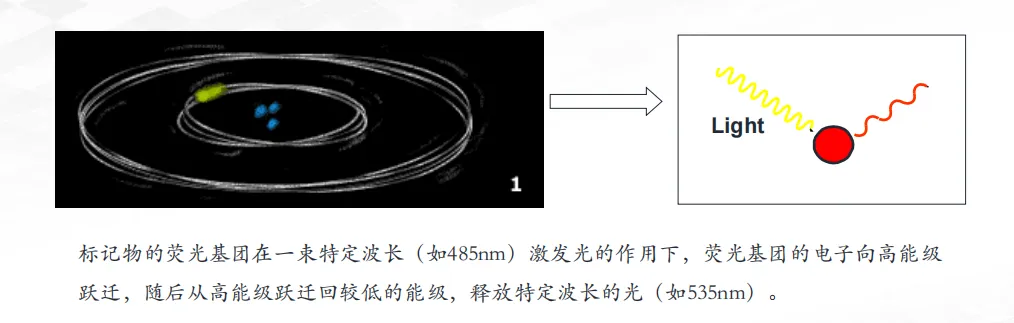
1.实验原理
荧光发光原理是通过使用荧光染料、探针或荧光蛋白,在特定波长的激发光照射下,发射出波长大于激发光波长的荧光信号。这种技术依赖于荧光基团在受到激发后,电子从基态跃迁到激发态,然后返回基态时释放能量,产生荧光。
2.实验步骤
将荧光报告基团/荧光染料标记的药物,注射入小鼠体内;
小鼠经过麻醉后放入成像暗箱平台,照明灯拍摄第一次背景;
照明灯自动关闭,暗场特定波长的激发光照射下,并收集对应波长的发射光波长的荧光信号。

荧光成像常用标记方法及染料
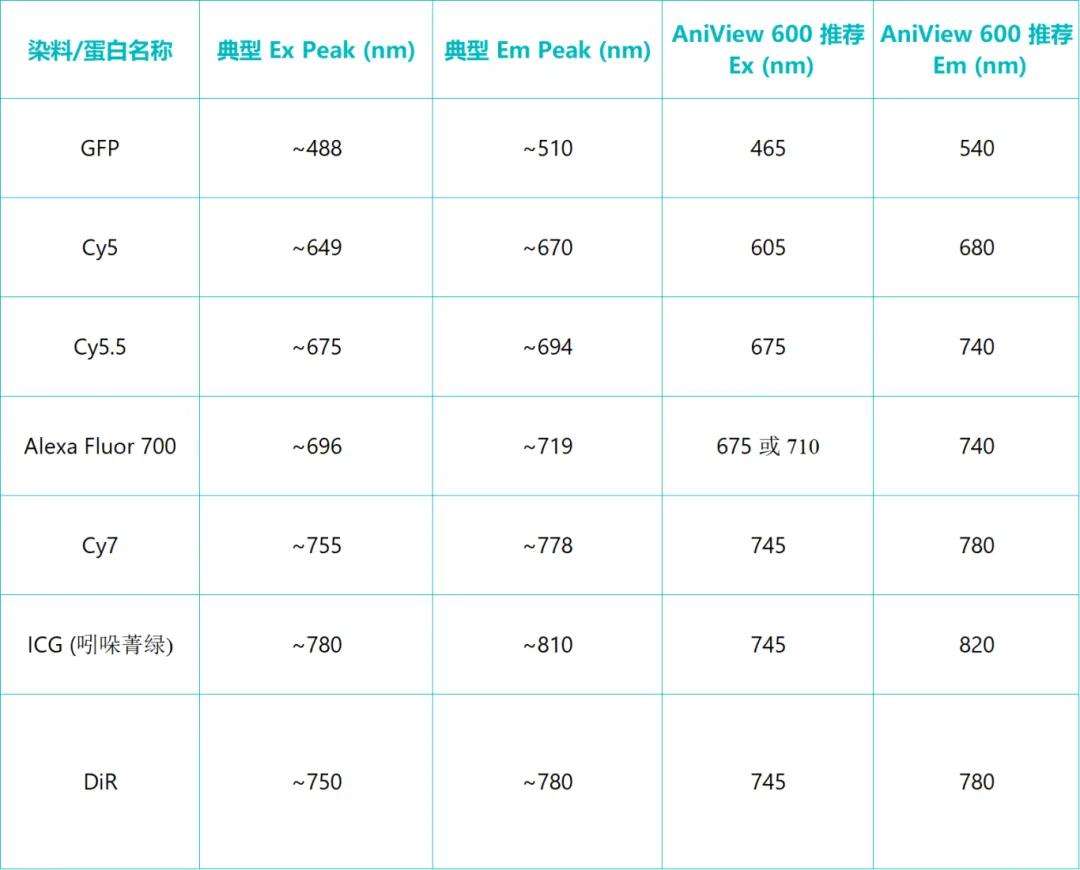
03实验设计避坑指南
完美的图像始于严谨的设计。以下关键点决定了实验的成败:
标记策略的选择: 注意ACQ(聚集淬灭) 与AIE(聚集诱导发光) 效应,避免信号假阴性。 小分子染料代谢快?可通过PEG化修饰或使用纳米载体延长循环时间。靶向性不足?在PEG层末端连接靶向分子(如叶酸、RGD肽、抗体),实现主动靶向至特定细胞。
图. PEG修饰示意图

图. RGD修饰示意图
材料选择-低波长染料:常见问题为体内材料荧光检测较低,全都是背景。尽量避免选择<600nm激发和发射的荧光染料。
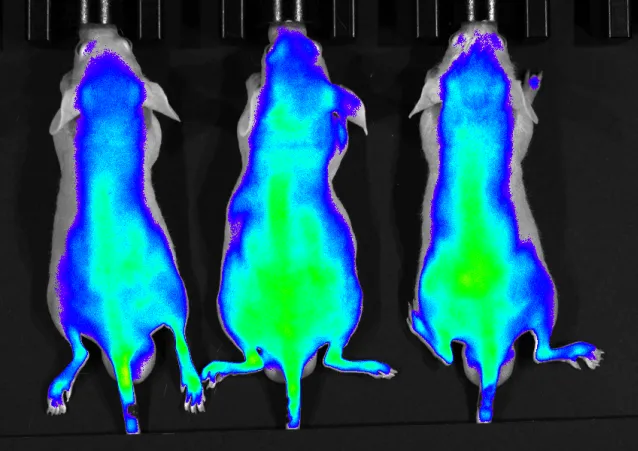
图. 低激发发射波长下的动物背景
动物准备是关键:务必脱毛!毛发是主要的背景荧光与散射来源,会严重干扰信号。
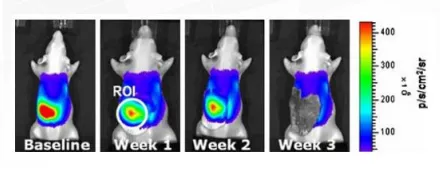
图. 动物毛发带来的荧光信号干扰
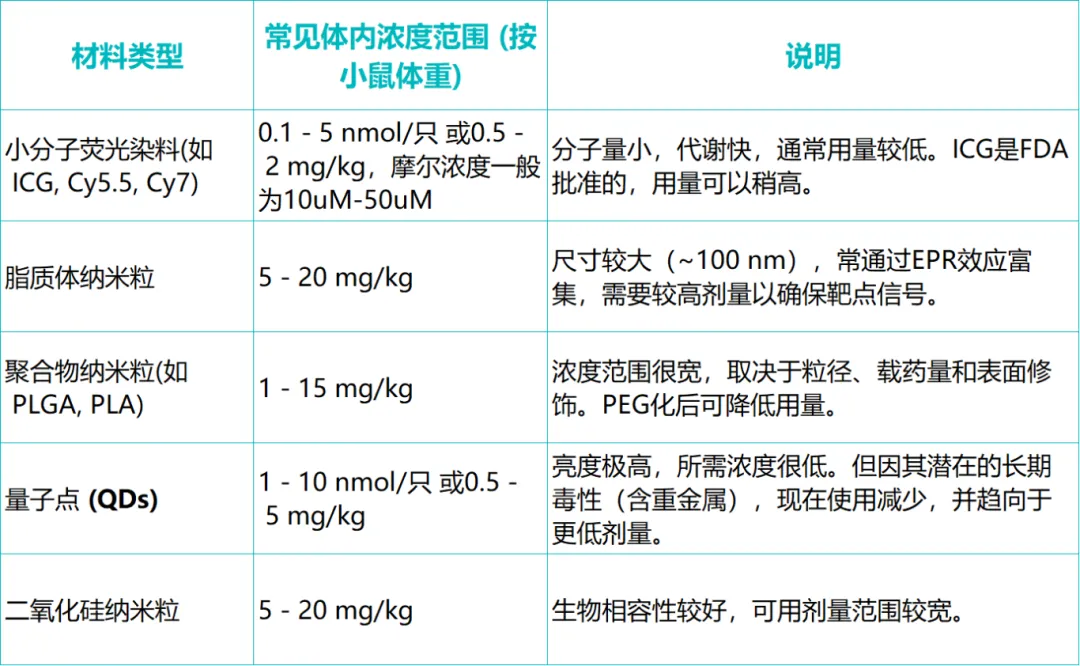
小动物活体成像,本质是一个系统工程,需要从模型、材料、成像参数到数据分析全流程协同。希望本文能为你的下一步研究提供清晰的指引。

活体成像9折优惠
扫码咨询了解
本文专享福利











 您已经拒绝加入团体
您已经拒绝加入团体

 2026-01-23
2026-01-23
 643
643
 0
0










