【摘要】 DC从外周组织迁移到传入淋巴管,然后迁移到引流淋巴结依赖于趋化因子的引导
树突状细胞(dcs)在连接先天免疫和适应性免疫中起着至关重要的作用。未成熟的树突状细胞作为外周组织的哨兵,特别是那些抗原暴露丰富的组织(如皮肤和粘膜表面)。在取样抗原后,它们可以经历激活和成熟过程,并通过传入淋巴管迁移到引流淋巴管。节点(LNs)。dc到达引流LNs后,向幼稚T细胞呈递抗原,刺激淋巴细胞扩增和分化[1]。
DC迁移是在维持免疫监视和组织稳态以及疾病发病过程中执行其功能的基础。这种迁移受到多种信号的严格调控,其中受体趋化因子轴起着重要作用。[3]C-C趋化因子受体7 (CCR7)及其两个配体,C-C趋化因子配体19 (CCL19)和CCL21,构成了主导的受体-趋化因子轴,参与了dc从外周部位向淋巴结的定向迁移。
其他轴,如C-XC趋化因子配体12 (CXCL12)及其受体C-X-C趋化因子受体4 (CXCR4),鞘氨醇-磷酸(S1P)和S1P受体,也参与了这一过程。更好地了解DC迁移对于成功地操纵DC和微调过敏治疗中的免疫反应以及开发有效的疫苗和癌症免疫疗法至关重要。

图1. DC向引流淋巴结迁移示意图[1]
DC从外周组织迁移到传入淋巴管,然后迁移到引流淋巴结依赖于趋化因子的引导(图1)。为了模拟DC在受限组织环境中的迁移,设计了BM-Chip(图2)。BMChip包括开放式储层,用于化学引诱剂和介质,以及具有三个高度的连接微流体网络:高20 μm、包含单细胞圈闭柱的中心细胞加载通道;高4 μm、宽5 μm、连接开放储层的正交受限迁移通道阵列;以及高150 μm、宽1.5 mm、连接开放储层的大型旁路/平衡通道。
每个芯片包含四列细胞陷阱(每列250个细胞陷阱)和五个大型水库,所有水库都通过旁路通道相互连接。该芯片是预功能化的人胶原I型模拟细胞外基质在体内。将单个细胞悬浮液装载到每个入口,并通过出口的负压流入中央通道。单细胞被v形挂钩捕获,形成均匀且可重复的高效单细胞柱。
为了获得较高的捕集效率,在前人的基础上对中心通道的宽度、圈闭的尺寸以及相邻两个圈闭之间的距离进行了优化。在装载细胞后,入口和出口被紧紧堵塞,以阻止在中央通道的流动。然后立即将趋化剂储存库中的培养基改为含有指定趋化因子的培养基。选择性细胞检索可以对具有不同趋化电位的细胞亚群之间的基因表达差异进行后续细胞分析或分子分析。
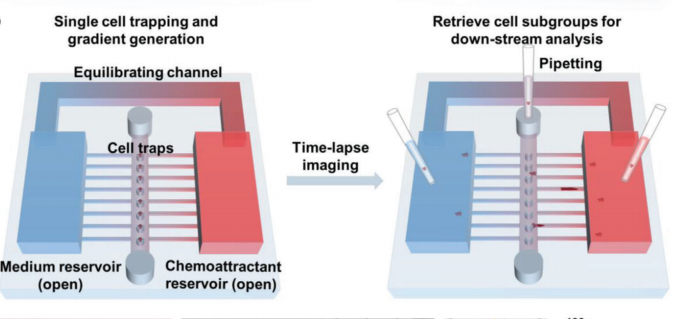
图2. 从细胞装载和梯度生成到迁移后的细胞回收的BM-Chip实验示意图[1]
[1] Shao N, Zhou Y, Yao J, et al. A Bidirectional Single‐Cell Migration and Retrieval Chip for Quantitative Study of Dendritic Cell Migration [J]. Advanced Science, 2023, 10.
科学指南针以分析测试为核心,提供材料测试、环境检测、生物服务、模拟计算、科研绘图等多项科研产品,累计服务1800+个高校、科研院所及6000+家企业,获得了60万科研工作者的信赖。始终秉持“全心全意服务科研,助力全球科技创新”的使命,致力于为高校、院所、医院、研发型企业等科研工作者提供专业、快捷、全方位的服务。
免责声明:部分文章整合自网络,因内容庞杂无法联系到全部作者,如有侵权,请联系删除,我们会在第一时间予以答复,万分感谢。











 您已经拒绝加入团体
您已经拒绝加入团体

 2024-12-31
2024-12-31
 5101
5101
 0
0










