【摘要】 PAI主要利用人类组织中发色团的固有光学吸收,如血红蛋白、黑色素、脂质和水。
光声(PA)成像(PAI)或光声成像是一种混合成像模式,融合了光学照明和超声(US)检测。在过去的二十年里,它在生物医学成像应用中迅速普及和探索。由于光学散射,纯光学成像方法无法在深层生物组织中保持高分辨率成像,因此在长达厘米深度的生物组织中实现高分辨率光学对比图像的能力使PAI成为各种临床成像应用的有前途的技术。在PAI中,通常使用纳秒脉冲激光(脉冲持续时间<10ns)照射生物样品。分子吸收光能并将其转化为热量,从而产生温度上升。由温度上升引起的热弹性膨胀产生声波,该声波使用超声波换能器进行检测。由于声音的散射比光小1000倍,声学信号在生物组织中传播得更长而没有显著衰减。
PAI主要利用人类组织中发色团的固有光学吸收,如血红蛋白、黑色素、脂质和水。由于这些发色团中的每一个都表现出自己的特征吸收光谱,多个波长的PAI允许它们的相对定量,并有助于研究疾病的生理变化,以了解它们背后的机制以及如何有效地管理它们。由于其无标签性质,它鼓励患者遵守规定,并能够进行长期纵向监测。由于PAI可以区分脱氧血红蛋白(Hb)和氧合血红蛋白(HbO2),因此测量血管中的sO2是可能的,这对于其他应用来说是缺血、缺氧或低氧血症生理状态的一个重要特征。
通常,根据光学照明方法和声学检测方法的组合,P. Beard等人[1]PAI系统可以分为三种配置:断层扫描、介观显微镜和显微镜系统(图1)。典型的光声层析成像(PAT)系统使用宽场照明,并通过单个元件或阵列换能器检测声波。单元件换能器的使用是时间密集型的,并且仅提供静态成像,使得其不足以用于体内临床成像应用。通过使用多个换能器进行检测,可以以多个角度捕获发射的声波,因此非常适合以提高的采集速度实时监测成像区域。

图1 光声成像系统的不同模式以及用于临床应用的商业系统的示意图。(a) 光学分辨率光声显微镜(OR-PAM)(b)光栅扫描光声介观显微镜(RSOM)和光声层析成像(PAT),配备(c)线性、(d)弯曲、(e)手持式球形换能器阵列。FB,纤维束;超声换能器阵列;超声波换能器。
有趣的是,M. Toi等人[2]的研究表明PAI获得血管氧合状态的能力已被证明在很大程度上有助于评估抗癌治疗引起的血管变化。紫杉烷化疗后,观察到肿瘤周围血管的相对血氧饱和度较低,表明缺氧(图2)。同时,更细的肿瘤内血管变得明显,这表明血液灌注增加,可能是由于化疗相关的间质血压降低导致血管正常化。
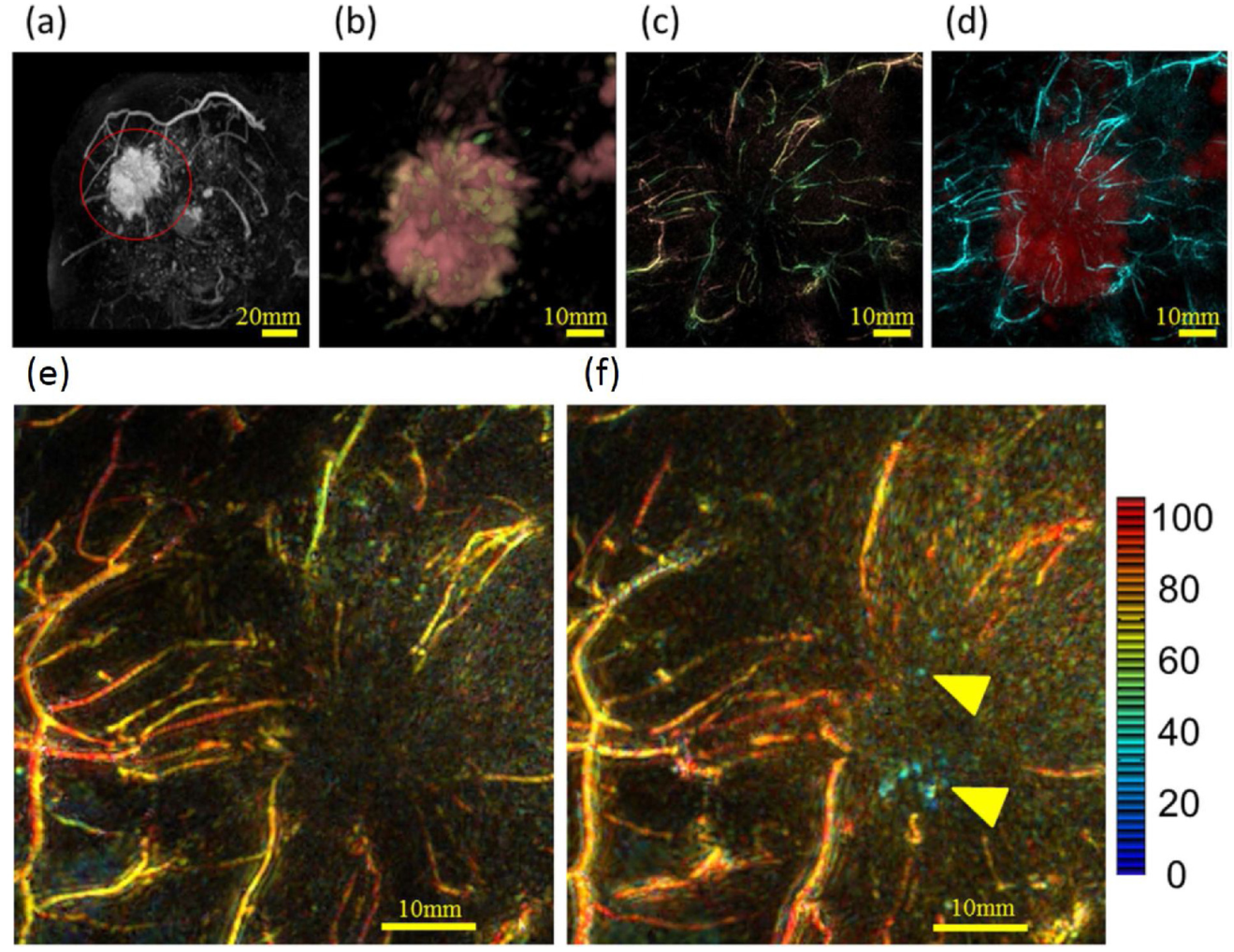
图2 一位40岁女性IBC肿瘤周围血管系统的PA乳腺镜图像。(a) 病变(直径47mm)的原始MR图像由红圈表示,(b)病变周围变形为PA图像形状后的放大MR图像,(c)原始PA图像,(d)融合的PA(青色)和MR(红色)图像,(e)795nm处的放大PA图像(表示血红蛋白分布)显示化疗前较小的肿瘤内血管,以及(f)795nm的放大PA图像显示化疗后肿瘤内较细血管数量增加。
[1] P. Beard, Biomedical photoacoustic imaging, Interface Focus 1 (4) (2011) 602–631.
[2] M. Toi, Y. Asao, Y. Matsumoto, H. Sekiguchi, A. Yoshikawa, M. Takada, M. Kataoka, T. Endo, N. Kawaguchi-Sakita, M. Kawashima, E. Fakhrejahani, S. Kanao, I. Yamaga, Y. Nakayama, M. Tokiwa, M. Torii, T. Yagi, T. Sakurai, K. Togashi, T. Shiina, Visualization of tumor-related blood vessels in human breast by photoacoustic imaging system with a hemispherical detector array, Sci. Rep. 7 (2017) 41970.
科学指南针在全国建立31个办事处和20个自营实验室,拥有价值超2.5亿元的高端仪器。检测项目达4000+项,覆盖材料测试、环境检测、生物服务、行业解决方案、模拟计算等九大业务。累计服务1800+个高校、科研院所及6000+家企业,获得了60万科研工作者的信赖。
免责声明:部分文章整合自网络,因内容庞杂无法联系到全部作者,如有侵权,请联系删除,我们会在第一时间予以答复,万分感谢。











 您已经拒绝加入团体
您已经拒绝加入团体

 2024-08-14
2024-08-14
 6915
6915
 0
0










