【摘要】 在许多情况下,水是理想的反应溶剂,可提供最佳产率和最快反应速率。
在点击化学反应家族中,最受关注的可能莫过于Cu(I)催化末端炔烃与有机叠氮化物发生1,3-偶极环加成反应(Huisgen反应)生成1,4-二取代1,2,3-三唑(方案1)。1 作为一种“好”的点击反应,该反应可靠、产量高、易于进行、不受空气或湿气的影响,并可兼容多种官能团。在许多情况下,水是理想的反应溶剂,可提供最佳产率和最快反应速率。通常情况下,环加成产物是固体,无需进行色谱纯化。1,2,3-三唑环化学性质稳定,不易水解、氧化、还原或以其他方式裂解。以上这些特性使得Cu(I)催化的叠氮-炔环化成为新药研发过程中药物分子库开发的重要手段。2
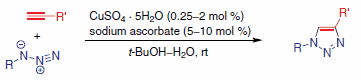
方案1
在抗坏血酸作为还原剂的条件下使用Cu(II)盐形成具有催化活性的Cu(I)一直是制备合成1,2,3-三唑的常选方法,但可能在生物偶联应用当中存在问题。Cu(I)盐,如[Cu(CH3CN)4]PF6可在稳定配体三[(1-苯甲基-1H-1,2,3-三唑-4-基)甲基]胺(TBTA)存在下直接使用(图1)。3 TBTA已被证明可以有效地增强铜催化的环加成反应,同时还不会破坏生物支架。
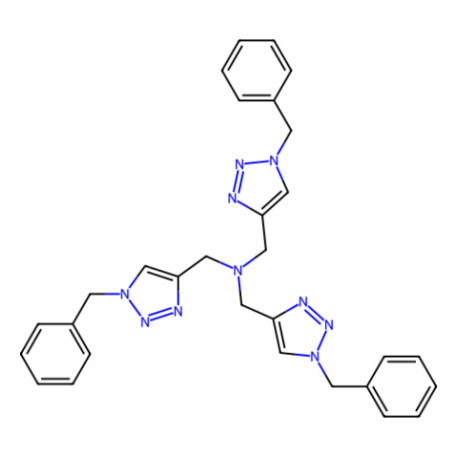
图1.TBTA
尽管Cu(I)催化的点击反应提供了获得1,4-二取代三唑的途径,但过渡金属变体获会得互补的1,5-二取代三唑异构体。在催化剂Cp*RuCl(PPh3)2的存在下,用叠氮化物处理末端或内部炔烃提供了具有完全控制区域特异性的高收率的环加合物(方案2)。4
方案2
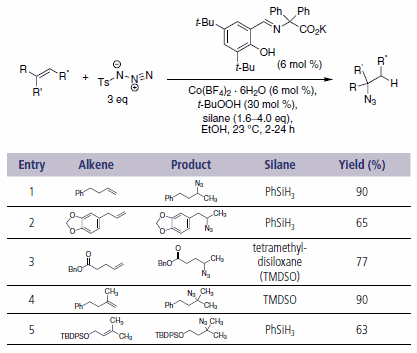
在市面上,许多有机叠氮化物是不易获得的。Carreira及其同事最近报道了Co(II)催化未活化烯烃与对甲苯磺酰基叠氮化物(TsN3)的加氢叠氮化反应,得到烷基叠氮化物(方案3)。5该催化剂很容易由Co(BF4)2·6H2O和Schiff碱配体原位制备。在加氢叠氮化反应中可以兼容单取代、二取代和三取代的烯烃,并且完全体现出马氏规则的选择性。此外,反应可以与夏普莱斯三唑环加成偶联,在一锅法中得到1,4-三唑。
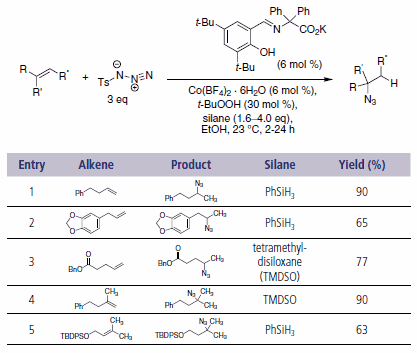
方案3
阿拉丁点击化学试剂 已上架科学指南针商城
创新、精选的试剂、催化剂与配体是加速点击化学反应研究、提升合成效率的核心驱动力。科学指南针商城现已全面上架阿拉丁高品质点击化学试剂产品,专为科研工作者在点击化学领域内的探索、开发直至工业化应用而精心打造。
下单链接:
阿拉丁三[(1-苯甲基-1H-1,2,3-三唑-4-基)甲基]胺:https://mall.shiyanjia.com/product-detail.html?product_id=149128&category=1
阿拉丁N -叠氮乙酰基甘露糖胺-四酰基化:https://mall.shiyanjia.com/product-detail.html?product_id=41055&category=1
阿拉丁无水醋酸铜:https://mall.shiyanjia.com/product-detail.html?product_id=146364&category=1
阿拉丁BTTAA:https://mall.shiyanjia.com/product-detail.html?product_id=8122&category=1
阿拉丁DBCO-PEG4-生物素:https://mall.shiyanjia.com/product-detail.html?product_id=937956&category=1
阿拉丁17-叠氮-3,6,9,12,15-五氧杂十七烷-1-胺:https://mall.shiyanjia.com/product-detail.html?product_id=1174&category=1
阿拉丁2-2-(2-叠氮基乙氧基)乙氧基:https://mall.shiyanjia.com/product-detail.html?product_id=136470&category=1
阿拉丁4-叠氮苯胺盐酸盐:https://mall.shiyanjia.com/product-detail.html?product_id=924444&category=1
阿拉丁甲氧基聚乙二醇叠氮化物:https://mall.shiyanjia.com/product-detail.html?product_id=24871&category=1
阿拉丁FAM叠氮化物,6-异构体:https://mall.shiyanjia.com/product-detail.html?product_id=83457&category=1
参考文献
1.Rostovtsev V. 2002. Angew. Chem.. Int. Ed.. 412596.
2.Tornøe CW, Christensen C, Meldal M. 2002. Peptidotriazoles on Solid Phase: [1,2,3]-Triazoles by Regiospecific Copper(I)-Catalyzed 1,3-Dipolar Cycloadditions of Terminal Alkynes to Azides. J. Org. Chem.. 67(9):3057-3064. https://doi.org/10.1021/jo011148j
3.Kolb H. 2001. Angew. Chem.,. Int. Ed. 402004.
4.Kolb HC, Sharpless K. 2003. The growing impact of click chemistry on drug discovery. Drug Discovery Today. 8(24):1128-1137. https://doi.org/10.1016/s1359-6446(03)02933-7
5.Manetsch R, Krasi-ski A, Radi-Z, Raushel J, Taylor P, Sharpless KB, Kolb HC. 2004. In Situ Click Chemistry: Enzyme Inhibitors Made to Their Own Specifications. J. Am. Chem. Soc.. 126(40):12809-12818. https://doi.org/10.1021/ja046382g













 2024-12-24
2024-12-24
 1062
1062
 0
0









