【摘要】 差热分析(DTA)原理:在程序控温条件下,测量试样与参比基准物质之间的温度差与环境温度的函数关系。
差热分析(DTA)
1. 差热分析的原理及设备
原理:在程序控温条件下,测量试样与参比基准物质之间的温度差与环境温度的函数关系。
操作方法:用两个尺寸完全相同的白金坩埚,一个装参比物,另一个装待测样品;将两只坩埚放在同一条件下受热,热量通过试样容器传导到试样内,使其温度升高,在试样内会形成温度梯度;温度的变化方式会依温度差热电偶接点处的位置而不同;温点插入试样和参比物中,或坩埚外的底部。
注意事项:DTA的严密理论要求,必须按照各个装置的特有边界条件、几何形状,进行热传递的理论分析。
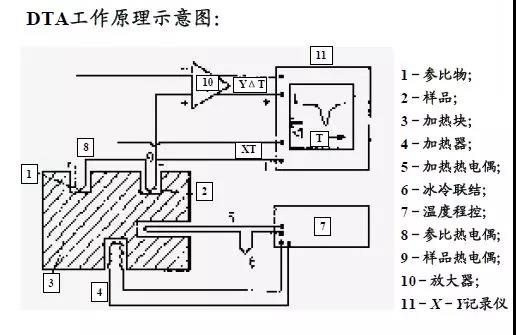
2.差热分析曲线
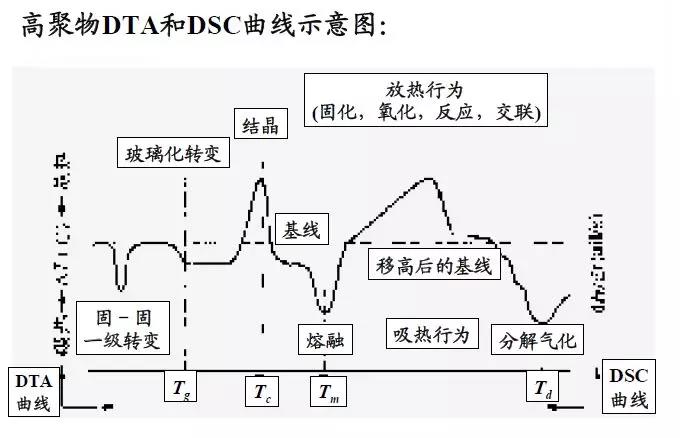
DTA曲线:以温度为横坐标、试样和参比物的温差ΔT为纵坐标,以不同的吸热和放热峰显示样品受热时的不同热转变状态
基线位置:ΔTa =(Cr- Cs)/K·Φ ( Φ = dTw/dt )
基线偏离零点的原因:试样和参比物之间的热容不等;故参比物最好采用与试样在化学结构上相似的物质,有时在试样中混些参比物来稀释,使Cr与Cs相近;K与装置的灵敏度有关,K增加,则ΔTa下降;升温速度Φ变化会影响基线,故须采用程序调节器以固定Φ.
测玻璃化温度的原理:试样在加热过程中热容变化,基线就会变动

仪器的灵敏度:常用措施,在样品容器和金属块之间留一个气隙,便可得到尖锐的峰.
实验进行到终点时,整个过程交换的热量:
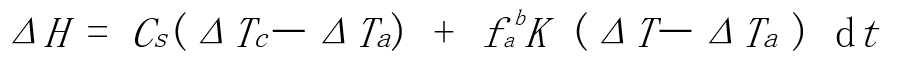
反应终点C的确定:
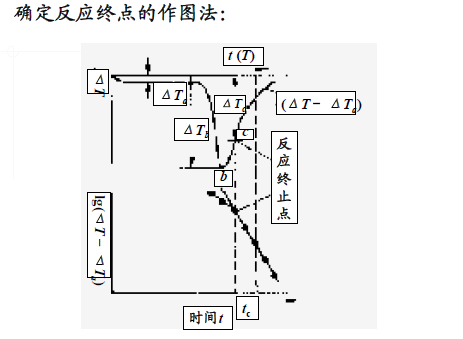
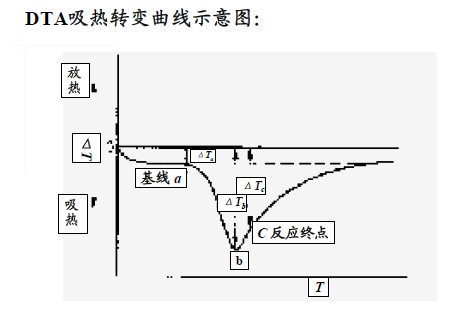
3. DTA测量应注意的要点及其影响因素
(1)注意程序控温的线性和速度;
(2)选择基准物时应考虑尽可能使Cr与Cs相近,使基线接近零线;
措施:选择在测量范围内本身不发生任何热变化的稳定物质,常用熔融石英粉、a-Al2O3和MgO粉末等;在试样与基准物的热容相差较大时,可用基准物稀释试样来加以改善
(3)测试过程中应注意水分干扰的影响,试样如果吸附一定的水分,将在100℃附近出现一个大的蒸发吸热峰干扰实验结果;
(4)测试过程中可会发生双峰交叠,应设法分峰;
(5)反应中的挥发物发生二次反应带来反应热的干扰;
(6)预结晶物质程序升温和降温曲线是不可逆的;
(7)DTA(包括DSC)需用标准物质校正测定温度的准确性,标准物质必须化学稳定,且蒸汽压低,故多数系金属盐类、纯金属或纯有机化合物
4. DTA的应用
凡是在加热(或冷却)过程中,因物理-化学变化而产生吸热或者放热效应的物质,均可以用差热分析法进行分析。
其主要应用范围如下:
(1)水
对于含吸附水、结晶水或者结构水的物质,在加热过程中失水时,发生吸热作用,在差热曲线上形成吸热峰。
(2)气体
碳酸盐、硫酸盐及硫化物等,在加热过程中由于CO2、SO2等气体的放出而形成吸热峰。不同类物质放出气体的温度不同,差热曲线的形态也不同,利用这种特征就可以对不同类物质进行区分鉴定。
(3)价态变化
材料中含有变价元素,在高温下由低价态变为高价态而放出热量,形成放热峰。变价元素不同,以及在晶格结构中的情况不同,则因氧化而产生放热效应的温度也不同。如Fe2+在340~450 ℃变成Fe3+
(4)重结晶
某些非晶态物质在加热过程中会发生重结晶而放出热量,在差热曲线上形成放热峰;晶态物质在加热过程中晶格结构被破坏,变为非晶态物质发生晶格重构,则也形成放热峰。
(5)晶型转变
有些物质在加热过程中由于晶型转变而吸收热量,在差热曲线上形成吸热峰。
四、DSC和DTA 的关系和区别
1. DSC和DTA 的关系
DSC的前身是差热分析(DTA)
差热分析(DTA)是在程序控制温度条件下,测量样品与参比物之间的温度差与温度关系的一种热分析方法。DTA输出的信号是温差(ΔT),而用温差来描述热量不但间接而且不够准确,难于进行热量的定量测定,无法建立△H与△T之间的联系。
差示扫描量热法 (DSC)是在程序控制温度条件下,测量输入给样品与参比物的功率差与温度关系的一种热分析方法,可以测试△T信号,并建立△H与△T之间的联系
2. DSC和DTA的区别
两种方法的物理含义不一样,DTA仅可以测试相变温度等温度特征点,DSC不仅可以测相变温度点,而且可以测相变时的热量变化。DTA曲线上的放热峰和吸热峰无确定物理含义,而DSC曲线上的放热峰和吸热峰分别代表放出热量和吸收热量。
DTA曲线上凸表示样品的温度比参比样品的温度高,下凹表示样品的温度比参比样品的温度低。DSC曲线上凸表示有热量释放出来,下凹表示有热量吸收,两者的趋势应该是大致一样。











 您已经拒绝加入团体
您已经拒绝加入团体

 2021-07-09
2021-07-09
 32174
32174
 1
1










