【摘要】 鉴于表面吸附和催化活性之间的强烈相关性,理想的催化剂基本上要求对反应物种具有适当的吸附强度,不是太强也不是太弱。

题目:通过d–d轨道调制优化氢气吸附以实现高效析氢催化
背景
鉴于表面吸附和催化活性之间的强烈相关性,理想的催化剂基本上要求对反应物种具有适当的吸附强度,不是太强也不是太弱。
由于Pt对于H合适的吸附活性,使其成为最受欢迎的HER催化剂,但其储量严重限制了该催化剂的进一步发展。
因此,开发具有类铂催化活性的非贵金属催化剂是非常重要的。其中揭示氢吸附和解吸行为的本质可以从根本上指导催化剂设计,提高催化性能。
研究思路及成果
He课题组通过金属二氧化钨(WO2)的d–d轨道相互作用系统地研究了氢吸附的调节。
理论模拟表明,后过渡金属原子(包括Fe、Co、Ni和Cu)的加入可以逐渐降低W-M位的键级,从而削弱氢吸附,加速析氢反应(HER)过程。在这一理论指导下,系统地筛选了各种3d金属掺杂WO2电催化剂的催化性能。
其中,Ni-WO2/泡沫镍的过电位为41 mV(-10 mA cm-2) 塔菲尔斜坡下降到47 dec-1代表迄今为止最好的钨基催化剂。这项工作表明,通过d–d轨道调制优化氢吸附是开发高效、稳定催化剂的有效途径。
结果与讨论
结构表征
为了探索d–d轨道耦合与催化性能之间的关系,作者选择WO2作为模型催化剂,通过引入一系列过渡金属杂原子来调节d轨道杂化(图1a)。
当Fe、Co、Ni或Cu金属杂原子取代其中一个W位并形成W-M键时,较高的d带填充原子坐标(3d 6至3d 10)将导致W-M键的反键轨道填充增加(图1b),并削弱键强度。
图1c很明显表明,WO2中W1 5d和W2 5d轨道的中心几乎重合,并显示出强烈的d–d轨道杂化,但随着杂原子的引入,W 5d和M 3d轨道之间存在线性解耦趋势。
从图1d可以看出,WO2中的W-W配位具有更大的键级值,这表明相邻两个W原子之间的相互作用很强。随着Fe、Co、Ni和Cu金属杂原子的引入,W-M键序逐渐降低,对应于配位强度的减弱。
值得注意的是,W-Cu的键级接近于零(0.01),实际键合可能不稳定。计算结果表明,在WO2晶格中引入金属杂原子可以通过调节W 5d-M 3d轨道杂化,有效地削弱W-M位上的氢吸附。
更有趣的是,氢吸附的吉布斯自由能(ΔGH*)和W-M配位之间存在火山关系,如图1e所示,其中,W-Ni构型对氢的吸附最温和,这可能使其成为一种优越的HER催化剂。
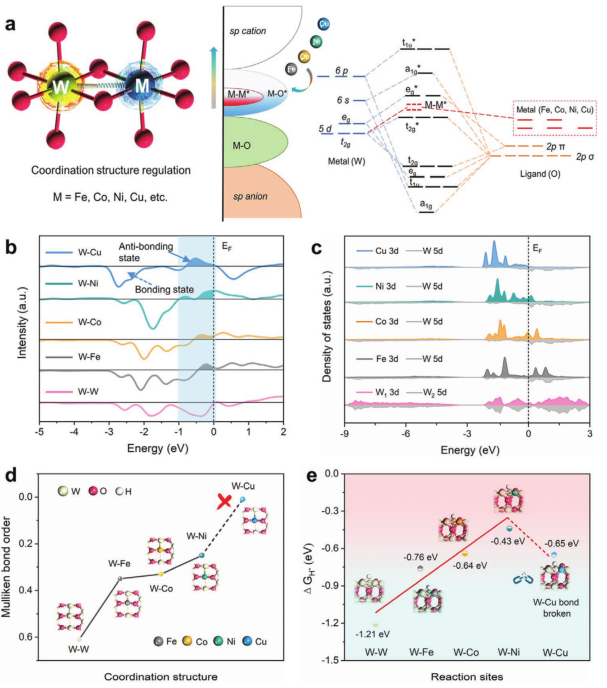
图1 配位结构和吸附能分析:a)M-WO2(M=Fe、Co、Ni、Cu等)的W 5d-M 3d轨道调制示意图。b)W-M键的晶体轨道哈密顿布居(COHP)分析。c)WO2中W-W和M-WO2中W-M的态密度(DOS)图。d)不同W-M构型对应的键极。e)计算了M-WO2(011)在不同反应位置上的氢吸附吉布斯自由能,M代表铁、钴、镍、铜等。
图2a中WO2和Ni-WO2的XRD图谱显示出非常相似的轮廓,由单斜结构的WO2组成。图2b表明在退火原始纳米线结构之后变得更加多孔。合成的镍掺杂WO2呈现多孔纳米线结构,TEM图像也进一步证实了这一点(图2c)。
图2d也可以观察到Ni-WO2的晶体结构,其中晶面间距晶格条纹为0.343nm,对应于WO2的(011)晶面。此外,图2e中的元素映射显示了W(黄色)、O(红色)和Ni(绿色)元素在整个多孔WO2 NW中的均匀分布。
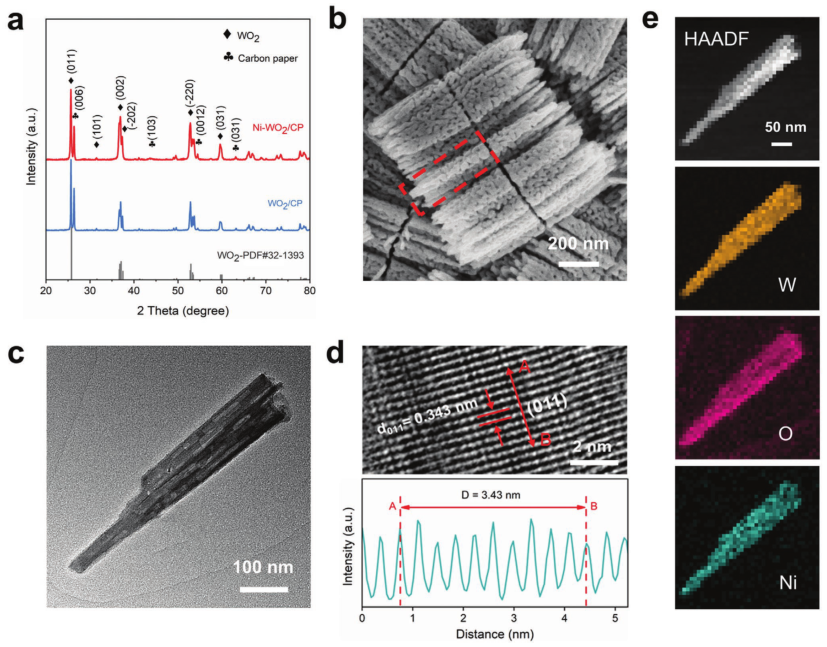
图2 Ni-WO2的形貌和结构分析。a)WO2和Ni-WO2的XRD图谱。b)Ni-WO2纳米线的SEM图像。c)Ni-WO2的TEM图像。d)Ni-WO2的HRTEM图像和相应的线扫描轮廓。e)Ni-WO2的HRTEM-HAADF图像和相应的EDS元素分布。
从图3a可以看出Ni-WO2的突出峰强度高于WO2或W箔,表明Ni-WO2中W元素的氧化电子结构。
此外,与WO2相比,Ni-WO2的显著峰位略微向高结合能区移动,表明Ni-WO2的W原子上的d带占据态减少,表明,Ni原子的引入可以有效地诱导W原子周围的电荷分布,从而降低W原子获得电子的能力。
从图3b-d中可以直观的看到其成键情况以及键长的变化,影响其W周围的电子分布,如图3e-f所示,最终表明与原始W-W键相比,Ni-W之间的电荷密度大大降低,导致与W-W相比,Ni-W两者之间的相互作用减弱。
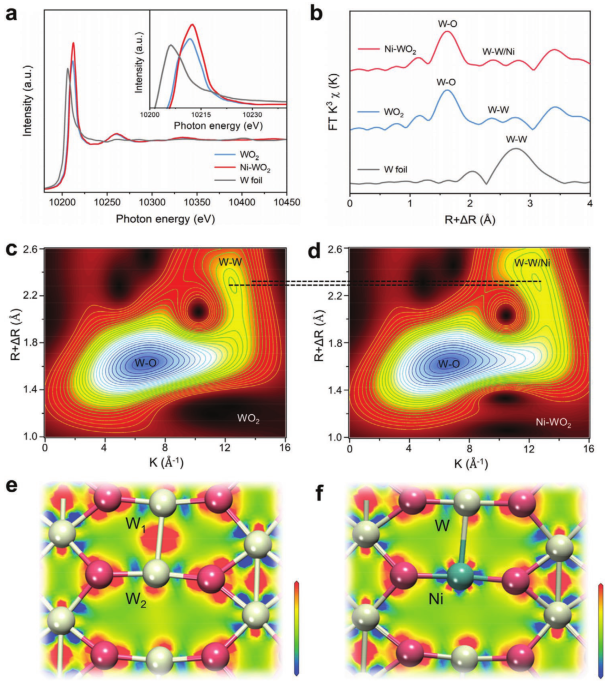
图3 电子结构和配位结构表征:a)归一化的W L3边缘XANES光谱(插图:放大的W L3边缘XANES光谱)。b) WO2、Ni-WO2和W箔的傅里叶变换EXAFS光谱的径向分布。c)WO2和d)Ni-WO2的小波变换的整体轮廓图。e)WO2(011)和f)Ni-WO2(011)的俯视电子密度差从-0.1到0.1 eÅ-3。
催化性能测试及机理分析
图4a表明制备的Ni-WO2/CP表现出最佳性能,最低过电位为83 mV(-10 mA cm-2) 在碱性条件下,甚至优于商用Pt。
从图4b可知其中Ni-WO2具有合适的键级、最适度的氢吸附和最佳的催化性能。作者通过循环实验测试,发现在-100 mA cm-2下循环100小时仍然具有很好的稳定性,且在2000次循环以后的极化曲线具有保持稳定,且优于其他对比的催化剂(图4c-d)。
显然,裸WO2对碱性HER几乎不起作用,而Ni掺杂WO2具有更有利的吸附能与WO2比(−R1-RC1为-0.94 eV和IM1′-RC2为-0.87 eV,过渡态势垒更小(RC1-TS1为0.18 eV,RC2-TS2为0.22 eV)。
此外,HO*(IM1到IM1′)从Ni-WO2催化剂表面的脱附更容易,因此另一个H2O分子可以很容易地占据空位W并形成RC2。
此外,水分解产生的氢被紧紧吸附在WO2表面,这可能会阻碍HER催化过程。幸运的是,Ni原子的引入可以通过调节Ni和W原子之间的电荷密度有效地削弱氢的吸附,从而赋予Ni-WO2优良的碱性HER活性。
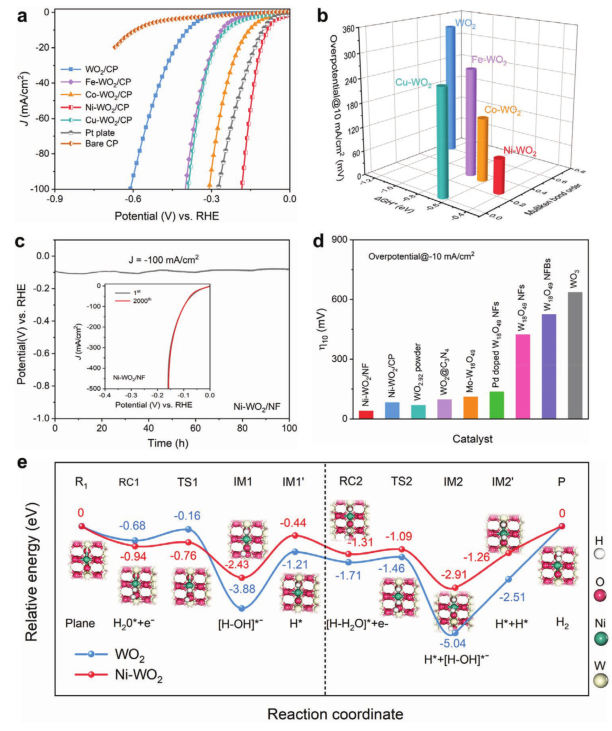
图4 催化剂性能和反应路径分析:a)WO2/CP、Fe-WO2/CP、Co-WO2/CP、Ni-WO2/CP、Cu-WO2/CP、Pt和裸CP在1.0 M KOH溶液中的LSV曲线。b)过电位、ΔGH*和Milliken键级之间的对应关系。c)Ni-WO2/NF在100小时电流密度下的长期稳定性试验-100 mA cm-2,插图是Ni-WO2/NF的初始极化曲线和第1000次极化曲线。d)Ni-WO2/CP和Ni-WO2/NF在室温下-100 mA cm-2下的过电位与最近报道的一些钨基氧化物HER电催化剂相比。e)沿着反应路径的各种反应物种的相对能量分布和简化表面结构,包括分别在WO2(011)和Ni-WO2(011)上碱性条件下的H*生成过程(左图)和H2生成过程(右图)。R:反应物;RC:反应物络合物;TS:过渡态;IM:中间体;P:产物。
本文所有内容文字、图片和音视频资料,版权均属科学指南针网站所有,任何媒体、网站或个人未经本网协议授权不得以链接、转贴、截图等任何方式转载。











 您已经拒绝加入团体
您已经拒绝加入团体

 2022-03-02
2022-03-02
 7724
7724
 0
0










