【摘要】 利用密度泛函理论,综合分析了氧空位对NiO(100)化学吸附态的影响,并进行了Bader电荷、电荷重分布和态密度分析。
空位缺陷是测定金属氧化物反应性的重要参数。催化、燃料电池、电池和其他能量转换技术(如化学环燃烧)等不同领域都可以从空位缺陷对金属氧化物反应性影响的基础研究中受益。
在Negar Manafi Rasi等人的工作中研究了氧空位对NiO反应性的影响,NiO是上述领域中一个很有前途的材料。利用密度泛函理论,综合分析了氧空位对NiO(100)化学吸附态的影响,并进行了Bader电荷、电荷重分布和态密度分析。
H2在吸附时给电子到表面,而O空位的加入使得H2给电子到表面的数量增加,从而形成更稳定的状态。
虽然这似乎与产生O空位后表面变得富集电子相反,但推测,电子给予的增加是由于H与表面相互作用的变化以及NiO中的Ni和O的吸附位点从NiO中的O和O空位变为NiO1- x中的O和O空位。
计算了NiO和NiO1的吸附H、吸附位点、表面和亚表面(第二层)层的Bader电荷。计算值如表1所示。
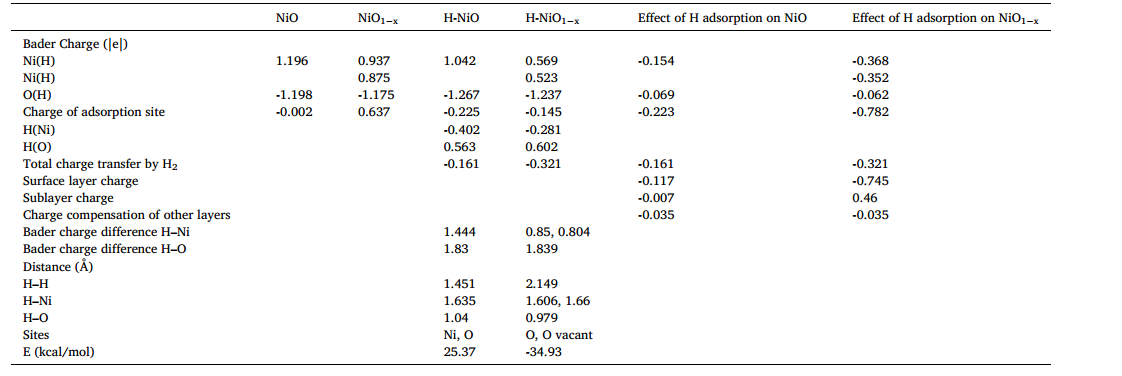
表1 NiO、NiO1- x、H-NiO和H-NiO1 - x的Bader电荷比较[1]
这将在Bader、电荷重分配和DOS分析的帮助下进一步研究。通过包含一个氧空位,吸附位点从NiO上的Ni和O位点转变为NiO1上的O和O空位。带正电的氧空位上吸附的氢与两个相邻的Ni原子的相互作用增强。
结果表明,H-Ni相互作用强度的变化是O空位加入后NiO反应性增强的主要原因。这些结果建立了对通过产生O空位来增强反应性的理解,并阐明了空位导致的键合性质的变化。
贝德电荷分析的结果也使我们对相互作用的电负性和极性有了更深入的了解。研究发现,H2通过O空位的加入而使其化学吸附状态更稳定,并向表面提供更多电子的原因是吸附位点的改变以及由此引起的氢与表面相互作用的改变。
相互作用变化的主要原因是氢在带正电的氧空位上的吸附和氢与相邻两个Ni原子的相互作用增强。电荷重分配分析发现,H和Ni原子之间的电子富集区增加,证实了Ni-H相互作用的共价增强。
DOS分析表明,在O空位形成后,H轨道的形状与Ni轨道的形状相似,再次证实了H与Ni之间的重叠和相互作用增强。
此外,由于O空位的加入,氢键轨道向低能态的转移,使得NiO1 - x的吸附态比NiO更稳定。分析表明,在O空位的加入下,氢氧相互作用没有明显的变化。O空位对氢吸附态贝德电荷和态密度的影响可以在今后的工作中进一步研究。
此外,由于空间位阻效应,在吸附位点有多个H2分子会影响表面的电子相互作用,这可以作为未来进一步研究的考虑因素。
[1]Rasi N M, Ponnurangam S, Mahinpey N. First-principles investigations into the effect of oxygen vacancies on the enhanced reactivity of NiO via Bader charge and density of states analysis[J]. Catalysis Today, 2023, 407: 172-181.
科学指南针充分发挥互联网技术和业务优势,在国内率先打造出业界领先的线上化、数字化的科研服务基础设施,在行业内首创用户自主下单、服务全流程追踪、测试“云现场”等模式,进一步提高了大型科学仪器设施开放共享和使用效率,以实际行动助力科技创新。现已发展成为中国专业科研服务引领者,已获得检验检测机构资质认定证书(CMA)、实验动物使用许可证、“ISO三体系认证”等专业认证。
免责声明:部分文章整合自网络,因内容庞杂无法联系到全部作者,如有侵权,请联系删除,我们会在第一时间予以答复,万分感谢。











 您已经拒绝加入团体
您已经拒绝加入团体

 2025-02-26
2025-02-26
 6136
6136
 0
0










